
TL;DR:
- Peptydy to krótkie łańcuchy aminokwasów o różnych długościach i funkcjach biologicznych.
- Budowa chemiczna i modyfikacje chemiczne wpływają na stabilność, biodostępność i skuteczność peptydów.
- Znajomość chemii peptydów pozwala świadomie wybierać produkty i poprawia skuteczność suplementacji.
Peptydy są powszechnie obecne w dyskusjach o suplementacji sportowej, regeneracji i zdrowiu, jednak zdecydowana większość aktywnych fizycznie osób nie potrafi precyzyjnie opisać ich chemicznej natury. Ta luka wiedzy ma realne konsekwencje: wybór nieodpowiedniego peptydu, błędne oczekiwania co do efektów lub nieświadome stosowanie preparatów o niskiej biodostępności. Zrozumienie, jak zbudowane są peptydy na poziomie molekularnym, pozwala podejmować trafniejsze decyzje suplementacyjne, lepiej interpretować etykiety produktów i świadomie oceniać ich potencjalne działanie. W tym artykule zostanie omówiona budowa peptydów, rodzaje aminokwasów, mechanizm powstawania wiązań peptydowych oraz praktyczne przełożenie tej wiedzy na cele fitness.
| Punkt | Szczegóły |
|---|---|
| Budowa peptydów | Peptydy to krótkie łańcuchy aminokwasów połączone stabilnym wiązaniem peptydowym. |
| Znaczenie struktur aminokwasów | Grupy R aminokwasów decydują o właściwościach i aktywności biologicznej peptydów. |
| Praktyczne zastosowanie | Wiedza chemiczna pozwala lepiej dopasować suplementację do indywidualnych celów treningowych i regeneracji. |
| Stabilność i biodostępność | Stabilność wiązania peptydowego wpływa na efektywność i trwałość suplementów. |
Skoro temat peptydów budzi tyle emocji w sporcie i zdrowiu, warto od podstaw zrozumieć, czym dokładnie są te związki. Zgodnie z definicją biochemiczną, peptydy to krótkie łańcuchy aminokwasów zazwyczaj liczące od 2 do 50 reszt aminokwasowych, połączonych wiązaniami peptydowymi. To właśnie ta zwięzłość struktury odróżnia je od białek, które są znacznie dłuższymi polimerami aminokwasowymi.
Klasyfikacja peptydów opiera się przede wszystkim na długości łańcucha. Szczegółowy podział według liczby aminokwasów/01%3A_Unit_I-_Structure_and_Catalysis/03%3A_Amino_Acids_Peptides_and_Proteins/3.01%3A_Amino_Acids_and_Peptides) wygląda następująco: oligopeptydy zawierają do 10-20 reszt aminokwasowych, polipeptydy do 50 reszt, a struktury powyżej tej granicy (lub o masie powyżej ok. 10 kDa) klasyfikuje się jako białka.
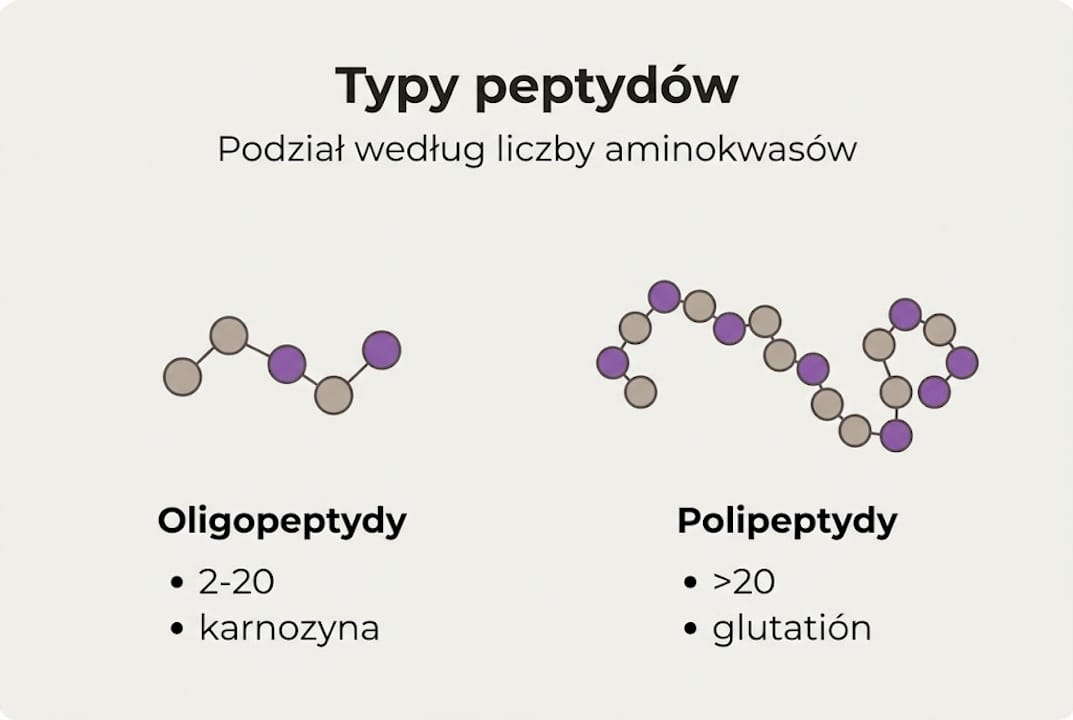
| Typ | Liczba aminokwasów | Przykłady |
|---|---|---|
| Oligopeptyd | 2–20 | karnozyna, glutatión, oksytocyna |
| Polipeptyd | 21–50 | insulina, glukagon |
| Białko | powyżej 50 | albumina, kolagen |
Synteza peptydów zachodzi na dwa główne sposoby. W organizmie przebiega jako biosynteza rybosomalną, kontrolowana przez kod genetyczny, gdzie rybosomy łączą kolejne aminokwasy zgodnie z matrycą mRNA. W laboratorium i przemyśle farmaceutycznym stosuje się natomiast chemiczną syntezę fazowo-stałą (SPPS, ang. solid phase peptide synthesis), która umożliwia precyzyjne projektowanie sekwencji aminokwasowej i wprowadzanie modyfikacji niedostępnych w syntezie biologicznej.
Dlaczego długość łańcucha ma znaczenie? Krótsze peptydy, takie jak di- i tripeptydy, są wchłaniane w przewodzie pokarmowym szybciej i efektywniej niż dłuższe polipeptydy, ponieważ mogą być transportowane przez dedykowane transportery peptydowe (PepT1) bez uprzedniej hydrolizy. Dłuższe łańcuchy wymagają enzymatycznego trawienia, co wpływa zarówno na czas działania, jak i na biodostępność aktywnych fragmentów. Pełniejsze omówienie tych zagadnień zawiera przewodnik po peptydach dostępny na stronie BioPepta.
„Peptydy są badane jako potencjalne środki terapeutyczne ze względu na ich wysoką swoistość i stosunkowo niską toksyczność w porównaniu z małocząsteczkowymi lekami syntetycznymi.” — biochemia kliniczna
Warto zaznaczyć, że modyfikacje chemiczne wprowadzane podczas SPPS, takie jak pegylacja, acetylacja N-końca czy amidowanie C-końca, znacząco zmieniają właściwości farmakokinetyczne peptydu. Szczegółowe informacje o tym, jak kompozycja peptydów wpływa na wyniki treningowe, są omówione w dedykowanym artykule.
Mając orientację, czym są peptydy, czas zobaczyć, z jakiego budulca są zbudowane. Aminokwasy to organiczne związki chemiczne stanowiące monomery wszystkich peptydów i białek. Każdy aminokwas posiada centralny atom węgla alfa (Cα), do którego przyłączone są cztery grupy: aminowa (-NH₂), karboksylowa (-COOH), atom wodoru oraz charakterystyczna grupa boczna R. Jak wskazuje biochemia strukturalna, każdy aminokwas ma centralny atom węgla alfa/01%3A_Unit_I-_Structure_and_Catalysis/03%3A_Amino_Acids_Peptides_and_Proteins/3.01%3A_Amino_Acids_and_Peptides) połączony z grupą aminową, karboksylową, wodorem i grupą boczną R.
To właśnie różnorodność grup R decyduje o unikalnych właściwościach każdego aminokwasu. Grupy boczne mogą być:
| Aminokwas | Typ grupy R | Właściwość | Rola w peptydzie |
|---|---|---|---|
| Glicyna | Niepolarna | Hydrofobowa | Elastyczność łańcucha |
| Seryna | Polarna | Hydrofilowa | Wiązania wodorowe |
| Kwas glutaminowy | Kwaśna | Ładunek (-) | Rozpuszczalność |
| Lizyna | Zasadowa | Ładunek (+) | Oddziaływania jonowe |
| Prolina | Cykliczna | Specjalna | Usztywnienie struktury |
Hydrofobowość i hydrofilowość aminokwasów mają bezpośredni wpływ na sposób, w jaki peptyd składa się w przestrzeni trójwymiarowej oraz na jego rozpuszczalność w środowiskach wodnych. Peptydy o wysokiej zawartości hydrofobowych aminokwasów mogą wykazywać tendencję do agregacji w roztworach wodnych, co wpływa na ich formulację farmaceutyczną. Informacje o tym, jak skład peptydów w treningu przekłada się na wyniki, są szczególnie przydatne dla sportowców.
Porada profesjonalisty: Czytając skład produktu peptydowego, zwróć uwagę na obecność proliny w sekwencji. Peptydy zawierające prolinę są bardziej odporne na działanie peptydaz, co oznacza dłuższy czas działania i lepszą stabilność w środowisku biologicznym.
Znajomość korzyści zdrowotnych peptydów w kontekście konkretnych aminokwasów pozwala trafniej interpretować deklaracje producentów i oceniać potencjał biologiczny preparatu.

Znając składniki peptydu, zrozumienie sposobu ich połączeń to absolutna podstawa. Wiązanie peptydowe powstaje w wyniku reakcji kondensacji między grupą karboksylową jednego aminokwasu a grupą aminową drugiego, z jednoczesnym uwolnieniem cząsteczki wody. Zgodnie z biochemią strukturalną, wiązanie peptydowe to amidowe wiązanie C-N/01%3A_Unit_I-_Structure_and_Catalysis/03%3A_Amino_Acids_Peptides_and_Proteins/3.01%3A_Amino_Acids_and_Peptides) powstające właśnie w tej reakcji kondensacji.
Etapy powstawania wiązania peptydowego:
Wyjątkową cechą wiązania peptydowego jest jego planarna geometria wynikająca z rezonansu elektronowego. Elektrony z grupy karbonylowej są częściowo delokalizowane na atom azotu, co nadaje wiązaniu C-N częściowy charakter wiązania podwójnego. Powoduje to, że obrót wokół tego wiązania jest ograniczony, a cztery atomy tworzące wiązanie (Cα-CO-NH-Cα) leżą w jednej płaszczyźnie.
Badania potwierdzają, że wiązanie peptydowe wykazuje wyjątkową stabilność z czasem półtrwania wynoszącym około 7 lat przy pH 7 i temperaturze 25°C, co czyni peptydy wyjątkowo trwałymi strukturami chemicznymi.
W zdecydowanej większości przypadków wiązanie peptydowe przyjmuje konfigurację trans, w której grupy boczne sąsiednich aminokwasów znajdują się po przeciwnych stronach płaszczyzny wiązania. Wyjątkiem są wiązania poprzedzające prolinę, gdzie konfiguracja cis jest energetycznie dostępna i biologicznie istotna.
Kierunkowość łańcucha peptydowego ma fundamentalne znaczenie dla jego funkcji biologicznej. Łańcuch zawsze posiada wolną grupę aminową na jednym końcu (N-koniec) i wolną grupę karboksylową na drugim (C-koniec). Sekwencja aminokwasów jest zawsze zapisywana i odczytywana od N-końca do C-końca. Ta kierunkowość determinuje sposób rozpoznawania peptydu przez receptory i enzymy. Więcej o tym, jak biodostępność peptydów zależy od struktury chemicznej, wyjaśniono w dedykowanym materiale.
Porada profesjonalisty: Stabilność wiązania peptydowego przekłada się bezpośrednio na trwałość suplementu. Jednak w organizmie enzymy (peptydazy) rozkładają wiązania peptydowe znacznie szybciej niż wynika to z termodynamiki chemicznej. Dlatego modyfikacje chemiczne, takie jak D-aminokwasy czy cyklizacja peptydu, stosowane w nowoczesnych preparatach, mają na celu ochronę przed enzymatyczną degradacją i wydłużenie czasu działania. Pełne omówienie mechanizmów działania peptydów dostępne jest na stronie BioPepta.
Po zgłębieniu zaawansowanej strony chemii czas na praktyczne przełożenie poznanej wiedzy na życie codzienne osoby aktywnej. Znajomość budowy chemicznej peptydów nie jest wiedzą wyłącznie akademicką, lecz ma bezpośrednie zastosowanie przy wyborze suplementacji.
Najlepiej zbadane przykłady peptydów stosowanych przez sportowców to karnozyna i glutation. Karnozyna to dipeptyd złożony z beta-alaniny i histydyny, obecny w wysokich stężeniach w tkance mięśniowej. Glutation to tripeptyd zbudowany z glutaminianu, cysteiny i glicyny. Jak wskazują dane biochemiczne, karnozyna i glutation wspierają buforowanie pH i zdolności antyoksydacyjne mięśni, co bezpośrednio przekłada się na opóźnienie zmęczenia i ochronę komórek przed stresem oksydacyjnym.
| Peptyd | Budowa | Główna funkcja | Cel suplementacyjny |
|---|---|---|---|
| Karnozyna | Dipeptyd (β-Ala + His) | Buforowanie pH mięśni | Wytrzymałość, opóźnienie zmęczenia |
| Glutation | Tripeptyd (Glu + Cys + Gly) | Antyoksydacja | Regeneracja, ochrona komórkowa |
| BPC-157 | 15 aa | Gojenie tkanek | Regeneracja po kontuzjach |
| IGF-1 LR3 | 83 aa | Sygnalizacja anaboliczna | Budowa masy mięśniowej |
Chemiczna budowa peptydu bezpośrednio determinuje jego odporność na degradację enzymatyczną, szybkość wchłaniania i mechanizm działania. Krótkie peptydy (di- i tripeptydy) są wchłaniane aktywnie przez transporter PepT1 w jelicie cienkim, co zapewnia im wysoką biodostępność nawet przy doustnym podaniu. Dłuższe peptydy wymagają iniekcji lub specjalnych nośników, aby dotrzeć do miejsca działania w niezmienionej formie.
Najczęstsze błędy przy wyborze peptydów do suplementacji:
Więcej o tym, jak peptydy wpływają na masę mięśniową i redukcję tkanki tłuszczowej, a także jak stosować je w kontekście peptydów w kulturystyce, można znaleźć w materiałach edukacyjnych BioPepta.
Większość osób aktywnych fizycznie patrzy na peptydy wyłącznie przez pryzmat oczekiwanego efektu, pomijając fundamenty chemiczne, które ten efekt warunkują. To podejście prowadzi do rozczarowań: zakup preparatu o nieodpowiedniej długości łańcucha, złej drodze podania lub niezweryfikowanej czystości nie przyniesie oczekiwanych rezultatów, niezależnie od renomy nazwy handlowej.
Zrozumienie, dlaczego krótszy peptyd działa szybciej (ale niekoniecznie silniej), a peptyd zawierający D-aminokwasy jest odporniejszy na enzymy, pozwala oceniać produkty z merytoryczną precyzją. Przykład: sportowiec wybierający peptyd kolagenowy do regeneracji stawów powinien wiedzieć, że hydrolizy kolagenu do di- i tripeptydów zapewniają lepsze wchłanianie niż niehydrolizowane polipeptydy.
Kolejny aspekt to weryfikacja składu. Wiedza o tym, jakie aminokwasy powinny tworzyć dany peptyd, umożliwia ocenę, czy deklaracja producenta jest wiarygodna. Dostępność wyników analiz laboratoryjnych, takich jak HPLC czy spektrometria masowa, staje się wówczas realnym kryterium wyboru, a nie tylko marketingowym hasłem.
Porada profesjonalisty: Zawsze szukaj w składzie produktu peptydowego informacji o czystości (powyżej 98% to standard dla preparatów badawczych), sekwencji aminokwasowej oraz wyników analizy co wpływa na biodostępność. Brak tych danych to sygnał ostrzegawczy.
Gdy jesteś świadom chemii peptydów, kolejny krok to wybór odpowiedzialnego dostawcy, który dostarcza produkty spełniające rygorystyczne standardy jakościowe. Skuteczność peptydu zależy nie tylko od jego struktury chemicznej, lecz przede wszystkim od potwierdzonej czystości i zgodności sekwencji aminokwasowej.
BioPepta oferuje peptydy z jakością potwierdzoną badaniami laboratoryjnymi, w tym analizami HPLC i spektrometrią masową, które weryfikują zarówno czystość, jak i tożsamość chemiczną każdego preparatu. W ofercie dostępna jest również woda bakteriostatyczna do peptydów, niezbędna do prawidłowego przygotowania roztworów. Zanim podejmiesz decyzję suplementacyjną, zapoznaj się z pełną ofertą i materiałami edukacyjnymi dostępnymi na sprawdzone peptydy BioPepta.
Peptyd składa się z 2–50 aminokwasów, natomiast białko to dłuższy łańcuch przekraczający granicę peptydy-białka wynoszącą ok. 50–100 reszt aminokwasowych, zazwyczaj o masie powyżej 10 kDa.
Największy wpływ mają boczne grupy R, ponieważ decydują o rozpuszczalności, hydrofobowości, ładunku elektrycznym i aktywności biologicznej całego peptydu.
Wiązanie peptydowe jest chemicznie bardzo stabilne, z czasem półtrwania ok. 7 lat przy neutralnym pH, co sprzyja trwałości preparatów peptydowych przechowywanych w odpowiednich warunkach.
Należy sprawdzać skład, długość łańcucha i typy aminokwasów, ponieważ dobór rodzaju peptydu do celu jest kluczowym czynnikiem determinującym skuteczność suplementacji.